第1章:電気化学測定の「基準」を知る
1-1 電気化学測定でなぜ参照電極を使用するのか? その役割について
一般的には、「正極」と「負極」の2つの電極があれば電気化学反応を進めることができます。実際、多くの電解反応はこの2電極系で行われます。
しかし、もう少し詳しく見てみると、この2つの電極(作用電極と対極)間に電圧をかけても、その電位は両電極に分かれてしまいます。そのため、両電極の間の電位差は分かっても、それぞれの電極でどのような電位になっているかを直接知ることはできません。さらに、電解により溶液内で電子の移動が起こる(電流Iが流れる)と、溶液中での電子の動きにくさ(抵抗R)による電位降下(E = IR)が生じ、正確な電位を測定することが難しくなります。
では、どうすれば目的とする反応が起こる「作用電極」の電位を正確に知り、コントロールできるのでしょうか。電気化学測定や有機電解合成では、作用電極の電位を正確に制御することが非常に重要です。
1-2 電位の普遍的なものさし「SHE」:標準水素電極の仕組みと課題
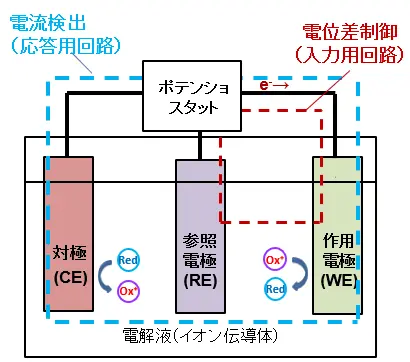
電位の基準となる電極は「参照電極(基準電極)」と呼ばれます。参照電極を理解する前に、電気化学測定に使われる「ポテンショスタット」という装置の主な機能を確認しておきましょう。
- 作用電極の電位を参照電極に対してコントロールする
- 作用電極に流れる電流を測定する
- 参照電極には電流を流さない
電気化学測定では、作用電極・対極・参照電極の3つを組み合わせて測定を行います。
ポテンショスタットは、参照電極の電位を基準にして、作用電極に常に指定した電位(例:+500 mVなど)がかかるように制御します。そのため、作用電極の電位を正確に制御するには、安定した普遍的な電位を持つ参照電極が必要になります。
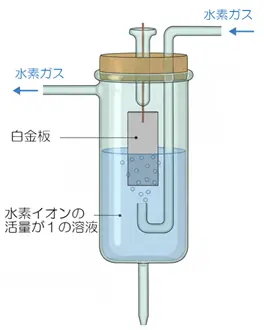
このとき基準として提案されるのが「標準水素電極(SHE: Standard Hydrogen Electrode)」です。
SHEは白金線をpH=0([aH+]=1 )の溶液に浸し、1 atmの水素ガスを常にバブリングすることで(図2)、普遍的な電位を保ちます。SHEを基準にすることで、さまざまな物質の電極反応電位を共通の基準で比較できるのです。
ただし、SHEは水素ガスの供給や安全管理などの運用が難しく、日常的な使用には不向きです。
1-3 実用的な参照電極の選び方:安定性と扱いやすさを兼ね備えた「二次標準」とは
SHEは理論的に最も安定した基準ですが、実際の測定では、SHEに対して既知の電位を持つ「二次標準参照電極(非分極性電極)」を使うのが一般的です(表1)。
電極名 構成・原理 標準電位(vs.SHE) 主な特徴 主な用途 SHE(標準水素電極) 白金+H2ガス+H+(a=1) 0.000 V 最も基本的な基準。運用が難しい。 基礎研究・校正用 RHE(可逆水素電極) 白金+H2+試料と同pH溶液 pH依存
(-59 mV/pH)液間電位差がない。pH依存系に便利。 電極反応機構の解析 Ag/AgCl電極 Ag/AgCl/KCl(飽和) +0.199 V
(飽和KCl)安定・取り扱い容易・非水銀 一般的な水溶液測定 カロメル電極 Hg/Hg2Cl2/KCl(飽和) +0.244 V 電位安定、ただし水銀使用 古典的測定・校正用 NaCl型Ag/AgCl電極 Ag/AgCl/NaCl溶液 +0.196 V
(3M-NaCl)KCl系より目詰まりしにくい。 過塩素酸系など特殊系 ※ SHEを除き、各参照電極の標準電位は温度や濃度に依存します。表中の値は25°Cでの代表値です。
水溶液系では、水素を使わず、内部の酸化体と還元体が平衡して電位を保つ電極が主に利用されます。
代表例として、銀塩化銀電極(Ag/AgCl電極)やカロメル電極があります。銀塩化銀電極で銀の表面では式1の様な可逆な酸化還元反応が起こっています。右向きが酸化反応、左向きが還元反応となります。これらが平衡している(両方向に同じ量で起こっている)ため、電位が安定し基準として使用する事が出来ます。
カロメル電極も電位が安定していますが、水銀を使用するため、環境面から現在は使用が減り、銀塩化銀電極が広く使われています。
当社では、外部からの衝撃に強いポリメチルペンテン樹脂製の電極ホルダーや、耐アルカリ性を高めたセラミック製の液絡部(多孔質のセラミック)を採用した参照電極を提供しています。また、内部液に塩化カリウム(KCl)だけでなく、塩化ナトリウム(NaCl)を使用した銀塩化銀電極もラインナップしています。
これは、使用環境に応じて長期的に安定した参照電極を選んでいただくためです。たとえば、燃料電池触媒評価などで過塩素酸を使用する場合、KClを内部液に使う電極では、溶解度の低いKClO₄(過塩素酸カリウム)が析出して液絡部が目詰まりするおそれがあります。その場合には、NaClを使用した「RE-1BP RE-1BP 水系参照電極(Ag/AgCl)」を選ぶと、長期間安定して測定を行えます。
また、SHEと類似した「可逆水素電極(RHE: Reversible Hydrogen Electrode)」もあります。
RHEは水素ガスを使う点は同じですが、内部溶液のpHが測定溶液と同じである点が異なります。RHEの電位はネルンスト式に従い、pH=0ではSHEと同じ電位を示しますが、pHが1上がるごとに電位はSHEから59 mV低下します。電位が変わることを懸念するかもしれませんが、pHが分かればネルンスト式で電位を正確に求められるため問題はありません。
RHEの利点は、測定溶液と同じpHの溶液を使うため、液間電位差が生じないことです。H⁺が関与する反応では、反応電位もpHに依存して変化します。たとえば、銀塩化銀参照電極を使って白金電極を負の方向にスキャンすると、酸性溶液ではすぐに水の分解(水素ガス発生)が起こりますが、アルカリ性ではより負の電位で分解が始まります。RHEでは、pHにより基準電位となる参照電極電位がネルンスト式に従いシフトする為、RHEに対する水が分解し始める電位が常に一定となります。この違いをイメージすると理解しやすいでしょう。
RHE基準で測定を行うと、水素発生や酸素還元(ORR)の電位をすぐに把握でき、サイクリックボルタンメトリー(CV)の電位走査範囲を設定しやすくなります。
第2章以降では、ここで紹介した各参照電極の特長に加えて、当社で取り扱う参照電極の選定方法、チェック方法、メンテナンス方法について紹介します。